Grados de diferenciación celular: qué dice el informe y por qué importa
Cuando un paciente recibe el resultado de una biopsia o de la anatomía patológica de una pieza quirúrgica, el informe rara vez es fácil de leer. Junto con el tipo histológico del tumor, aparecen términos como "bien diferenciado", "moderadamente diferenciado", "pobremente diferenciado" o expresiones como "G1", "G2", "G3", "Gleason 4+3" o "grado nuclear 2".
Estos términos describen el grado de diferenciación del tumor, una característica clínica con implicancias importantes para el pronóstico y para la planificación del tratamiento. Comprender qué significan ayuda al paciente a leer su propio informe con más claridad y a sostener una conversación más informada con el equipo oncológico.
Qué es la diferenciación celular
En el organismo, las células no nacen siendo lo que serán al final de su vida. Atraviesan un proceso progresivo de especialización que, partiendo de una célula muy básica, las lleva a adquirir las funciones específicas del tejido al que pertenecen. Una célula hepática, por ejemplo, recorre múltiples etapas de diferenciación hasta convertirse en un hepatocito maduro, capaz de cumplir con las funciones metabólicas, de detoxificación y de síntesis propias del hígado.
A medida que una célula se diferencia, ocurren dos cambios biológicos relevantes. Por un lado, la célula se vuelve estructuralmente más parecida al tejido sano de origen: adquiere las proteínas, las uniones intercelulares y la arquitectura propia de su linaje. Por otro lado, su tasa de reproducción (su capacidad de dividirse) disminuye. Una célula plenamente diferenciada cumple su función específica y se divide con baja frecuencia. Una célula poco diferenciada conserva un comportamiento más rudimentario, con alta tasa de mitosis.
En el contexto oncológico, la diferenciación de un tumor describe cuánto se parecen sus células al tejido sano del que se originaron. Esa comparación es la que da origen a los grados que aparecen en el informe.
Tres comportamientos clínicos diferentes
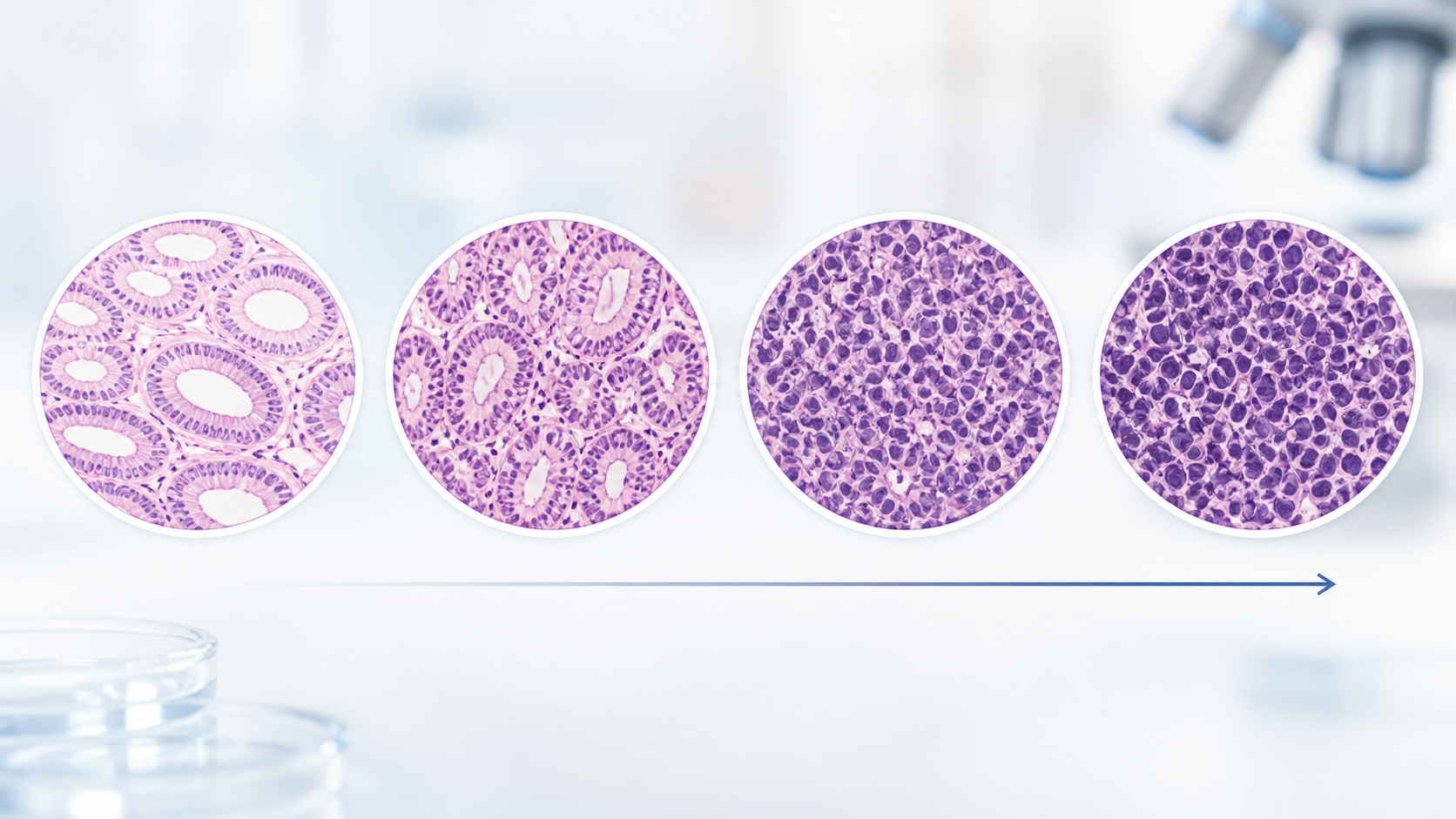
La anatomía patológica clasifica los tumores en una escala de diferenciación que tiene tres categorías principales, cada una con un comportamiento clínico característico.
Tumores bien diferenciados
Las células se asemejan a las células sanas del órgano de origen. Conservan estructura, organización tisular y uniones intercelulares fuertes. Su tasa de mitosis es baja: se dividen lentamente. Y al mantener una buena adhesión a las células circundantes, son menos propensas a desprenderse y migrar a distancia. En conjunto, estos tumores tienden a presentar menor agresividad y mejor pronóstico.
Tumores moderadamente diferenciados
Las células conservan rasgos del tejido original pero presentan zonas con uniones intercelulares incompletas. La adhesión es parcial. Se dividen con una tasa intermedia. Su comportamiento clínico es variable y se ubica entre los dos extremos.
Tumores pobremente diferenciados o indiferenciados
Las células se vuelven progresivamente más rudimentarias y pierden la mayoría de las características del tejido de origen. Dos cambios concurrentes definen su comportamiento: la tasa de mitosis aumenta considerablemente, y los puntos de adhesión entre células se debilitan. Esta combinación tiene una consecuencia clínica directa: las células se reproducen rápido y, al mismo tiempo, se desprenden con facilidad, lo que aumenta el riesgo de invasión local y de diseminación a distancia. Son los tumores de mayor agresividad.
Cómo se expresa esto en el informe
Para estandarizar la lectura, los patólogos utilizan sistemas de graduación que asignan un número a cada categoría. La nomenclatura más común utiliza la letra G seguida de un número:
- G1 corresponde a un tumor bien diferenciado.
- G2 corresponde a un tumor moderadamente diferenciado.
- G3 corresponde a un tumor pobremente diferenciado.
- G4 se reserva para tumores indiferenciados, en aquellos órganos donde se utiliza esta categoría.
- Gx indica que el grado no pudo ser determinado con la muestra disponible.
Cada órgano tiene, además, sistemas de graduación específicos que se ajustan a la biología particular del tejido. El score de Gleason se utiliza en cáncer de próstata y combina los dos patrones histológicos predominantes en una suma que va de 6 a 10. El sistema de Nottingham se aplica en cáncer de mama y evalúa tres parámetros (formación de túbulos, pleomorfismo nuclear y conteo mitótico) que se combinan en un grado final. Existen sistemas similares para riñón, sistema nervioso central, ovario y otros órganos.
La razón por la que existen sistemas distintos es simple: el comportamiento biológico de un tejido difiere del de otro, y la graduación se afina para reflejar esas diferencias. Por eso el informe anatomopatológico siempre debe leerse en el contexto del órgano de origen, junto con el equipo oncológico tratante.
Por qué la diferenciación condiciona el pronóstico
La relevancia clínica del grado de diferenciación se entiende a partir de los dos parámetros biológicos que ya describimos: tasa de mitosis y capacidad de adhesión.
La tasa de mitosis define la velocidad con que el tumor crece. Un tumor de baja tasa mitótica progresa más lentamente; un tumor de alta tasa mitótica puede duplicar su tamaño en períodos significativamente más cortos. Esto incide directamente en el ritmo de progresión clínica y en la urgencia con que se planifica el tratamiento.
La capacidad de adhesión define la probabilidad de que las células del tumor se desprendan del tejido primario y migren a otros órganos. La metástasis no es un fenómeno aleatorio: requiere que una célula tumoral se desprenda, sobreviva al tránsito por el torrente sanguíneo o linfático, y colonice un nuevo tejido. Las células con uniones intercelulares fuertes tienen menos probabilidad de iniciar este recorrido. Las células con adhesión débil, mayor probabilidad.
Por estas dos razones, el grado de diferenciación es uno de los factores que el oncólogo considera al estimar el pronóstico, junto con el estadio (extensión anatómica del tumor en el sistema TNM), el tipo histológico, los marcadores moleculares y otras variables clínicas.
Diferenciación no es destino
Conviene hacer una aclaración importante. El grado de diferenciación es un parámetro pronóstico, es decir, determina probabilidades, no certezas.
Existen tumores indiferenciados que responden muy bien al tratamiento, en parte precisamente porque su alta tasa de mitosis los vuelve más sensibles a los agentes que actúan sobre la división celular. Existen tumores bien diferenciados con comportamientos más persistentes de lo esperado. Y existen variables moleculares y biomarcadores que pueden modificar significativamente el escenario que sugiere el grado histológico aislado.
Por eso, el informe anatomopatológico es una pieza más dentro de un cuadro clínico más amplio. Su lectura aislada nunca alcanza para tomar decisiones. Su lectura integrada, junto con el resto de los estudios y la valoración del equipo tratante, es lo que permite definir el curso del tratamiento y estimar el pronóstico con la mayor precisión posible.
Lo que viene
Comprender por qué algunos tumores tienen alta tasa de mitosis y otros baja, y cómo se comportan las células según su grado de diferenciación, abre una pregunta natural: ¿cómo aprovechan los tratamientos oncológicos estas características?
La quimioterapia sistémica, en particular, está diseñada apuntando a dos mecanismos biológicos específicos que se vinculan directamente con lo que vimos en este artículo. Vamos a desarrollarlos en una próxima publicación.
Aviso médico
Este artículo tiene fines informativos y no reemplaza la consulta médica. La interpretación de un informe de anatomía patológica requiere una evaluación integral por parte del equipo oncológico tratante, considerando el tipo histológico, el estadio, los marcadores moleculares, el contexto clínico y los antecedentes del paciente. Ante cualquier duda sobre un informe propio, recomendamos discutirlo con el oncólogo de cabecera. Regemet no atiende urgencias: ante una emergencia, acuda al centro de salud más cercano.
Referencias
- Hanahan D, Weinberg RA. Hallmarks of Cancer: The Next Generation. Cell. 2011;144(5):646-674. Link
- Rakha EA, Reis-Filho JS, Baehner F, et al. Breast cancer prognostic classification in the molecular era: the role of histological grade. Breast Cancer Research. 2010;12(4):207. Link
- Henson DE, Chu KC, Levine PH. Histologic grade, stage, and survival in breast carcinoma: comparison of African American and Caucasian women. Cancer. 2003;98(5):908-917. Link
- Sun Z, Aubry MC, Deschamps C, et al. Histologic grade is an independent prognostic factor for survival in non-small cell lung cancer: an analysis of 5018 hospital- and 712 population-based cases. The Journal of Thoracic and Cardiovascular Surgery. 2006;131(5):1014-1020. Link
- Epstein JI, Egevad L, Amin MB, et al. The 2014 International Society of Urological Pathology (ISUP) Consensus Conference on Gleason Grading of Prostatic Carcinoma: Definition of Grading Patterns and Proposal for a New Grading System. The American Journal of Surgical Pathology. 2016;40(2):244-252. Link
- Pierorazio PM, Walsh PC, Partin AW, Epstein JI. Prognostic Gleason grade grouping: data based on the modified Gleason scoring system. BJU International. 2013;111(5):753-760. Link
- Onder TT, Gupta PB, Mani SA, Yang J, Lander ES, Weinberg RA. Loss of E-Cadherin Promotes Metastasis via Multiple Downstream Transcriptional Pathways. Cancer Research. 2008;68(10):3645-3654. Link
- Loh CY, Chai JY, Tang TF, et al. The E-Cadherin and N-Cadherin Switch in Epithelial-to-Mesenchymal Transition: Signaling, Therapeutic Implications, and Challenges. Cells. 2019;8(10):1118. Link
- Amin MB, Greene FL, Edge SB, et al. The Eighth Edition AJCC Cancer Staging Manual: Continuing to build a bridge from a population-based to a more "personalized" approach to cancer staging. CA: A Cancer Journal for Clinicians. 2017;67(2):93-99. Link
